Wat zijn edelgassen?
De edelgassen zijn de gassen helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe) en radon (Rn) uit groep 18 van het periodiek systeem.
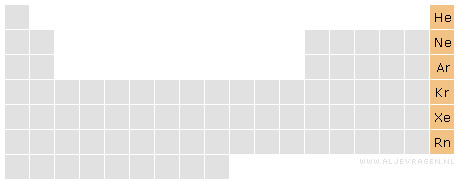
Edelgasconfiguratie
Een eigenschap van edelgassen is dat ze niet of nauwelijks reageren met andere stoffen. Deze zeer geringe reactiviteit wordt veroorzaakt door de stabiele elektronenomringing. Uit de elektronenconfiguratie blijkt dat edelgassen nul valentie-elektronen hebben. Er zijn dus geen elektronen beschikbaar om een gemeenschappelijk elektronenpaar te vormen met een ander atoom. Er zal dan ook geen reactie optreden. De elektronenconfiguratie van een edelgasatoom wordt ook wel de edelgasconfiguratie genoemd.
Toepassingen
De toepassing van edelgassen in het dagelijks leven hangt nauw samen met het gebrek aan reactiviteit.
Voorbeelden
- gas in een luchtballon (He)
- neonverlichting (Ne)
- gloeilampvulling (Ar)
  |
| Enkele voorbeelden van het gebruik van edelgassen in de praktijk: helium in een zeppelin en neonverlichting. |